신경계 중환자실에서 기계호흡 그래프 파형 감시와 분석
Monitoring and Interpretation of Mechanical Ventilator Waveform in the Neuro-Intensive Care Unit
Article information
Trans Abstract
Management of mechanical ventilation is essential for patients with neuro-critical illnesses who may also have impairment of airways, lungs, respiratory muscles, and respiratory drive. However, balancing the approach to mechanical ventilation in the intensive care unit (ICU) with the need to prevent additional lung and brain injury, is challenging to intensivists. Lung protective ventilation strategies should be modified and applied to neuro-critically ill patients to maintain normocapnia and proper positive end expiratory pressure in the setting of neurological closed monitoring. Understanding the various parameters and graphic waveforms of the mechanical ventilator can provide information about the respiratory target, including appropriate tidal volume, airway pressure, and synchrony between patient and ventilator, especially in patients with neurological dysfunction due to irregularity of spontaneous respiration. Several types of asynchrony occur during mechanical ventilation, including trigger, flow, and termination asynchrony. This review aims to present the basic interpretation of mechanical ventilator waveforms and utilization of waveforms in various clinical situations in the neuro-ICU.
서 론
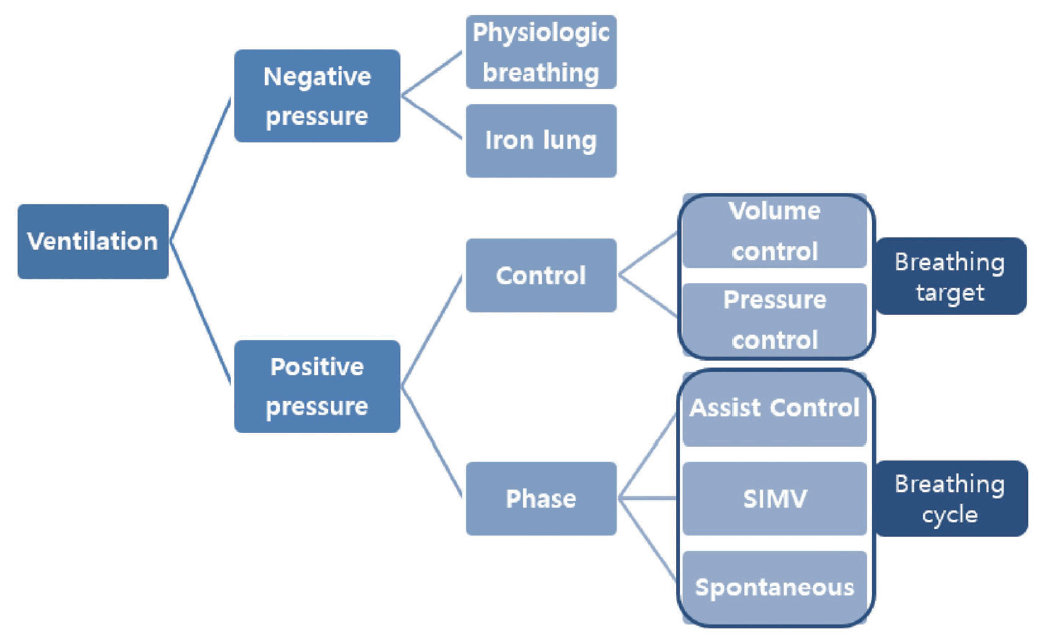
신경계 중환자실에서 기계환기(mechanical ventilation)는 중요하고 필수적인 보존적 치료 중 하나이다. 중환자실 입원이 필요한 뇌손상 환자에서 침습적 기계환기기(mechanical ventilator, 또는 인공호흡기)의 적응증은 1) 의식 저하에 의한 기도 확보, 2) 뇌손상과 관련된 폐손상 치료, 3) 불규칙한 호흡의 보조로 크게 나눌 수 있다. 기도, 폐손상, 호흡중추의 손상, 호흡근 마비 등 원인이 다르더라도 기계환기의 목적은 환자의 호흡부전이 해결될 때까지 산소화(oxygenation) 및 환기(ventilation)를 유지하며 호흡일(work of breathing)을 감소시키는 것이다(Fig. 1). 그러나 생리적 호흡과 다른 기계환기의 특성상 잘못 적용되면 오히려 기계호흡 유발 폐손상(ventilator induced lung injury, VILI)을 초래할 수 있다. 그러므로 폐손상을 최소화하기 위하여 처음부터 적절한 기계환기기 설정을 하고 환자에게 잘 적용되고 있는지 지속적인 감시와 조정이 필요하다. 환자와 기계환기기 사이의 지속적인 감시는 기계환기기에서 보여주는 수치와 그래프 파형(waveform)으로 인하여 얻을 수 있는 다양한 정보를 통하여 가능하다. 특히 신경계 중증질환의 환자는 뇌손상과 관련된 폐손상이 흔하고[1], 폐손상이 악화될 경우 저산소화 및 고/저탄산혈증(hyper/hypocapnia)에 의하여 뇌손상이 악화될 수 있으며[2], 일반적인 중환자와 달리 두개내압 상승이나 호흡중추 손상에 의하여 불규칙한 자발호흡으로 환자-기계환기의 비동시성(asynchrony, 또는 dyssynchrony)이 자주 관찰되기 때문에 기계환기기 그래프 파형의 의미를 아는 것이 신경계 중환자 관리에 도움이 된다. 본 종설에서 신경계 중환자실에서 기계환기를 적용한 환자에서 기계환기기 그래프 파형의 감시와 이에 따른 치료적 접근에 대하여 살펴보도록 하겠다.

Indications and simplified strategies of mechanical ventilation in neuro-ICU. GBS, Guillain-Barre syndrome; IICP, increased intracranial pressure; ARDS, acute respiratory distress syndrome; MG, myasthenia gravis; CIP, critical illness polyneuropathy; CIM, critical illness myopathy; FiO2, fraction of inspired oxygen; PEEP, positive end expiratory pressure; SBT, spontaneous breathing trial; SAT, spontaneous awakening trial; ICU, intensive care unit.
본 론
1. 기계환기 양식에 따른 기본 그래프 파형
기계환기의 양식(ventilator mode)은 통제변수인 제한(limit or target, 흡기의 목표)에 따라 용적조절환기(volume controlled ventilation, VCV)와 압력조절환기(pressure controlled ventilation, PCV)로 나누어지고, 호흡주기를 결정하는 위상변수(phase)인 유발(trigger, 흡기의 시작), 제한(흡기 시간), 주기(cycle, 흡기의 종료)에 따라 기계적조절환기(controlled mechanical ventilation, CMV), 보조조절환기모드(assist control mode ventilation [ACMV] 또는 assist control ventilation [ACV]), 동시성간헐필수환기(synchronized intermittent mandatory ventilation, SIMV)로 나누어진다(Fig. 2). 유발은 호흡주기의 시작을 결정하는 인자로 환자의 자발호흡 노력에 의하여 생기는 환자-기계환기기 기도내 압력 또는 유량의 변화를 기계환기기가 감지하여 시작하며 환자의 호흡 노력이 없으면 기계에 설정한 호흡수 대로 호흡이 이루어진다. 환자의 흡기 노력에 의하여 변하는 압력 또는 유량의 정도를 높이거나 낮추면서 기계환기가 시작하는 유발 민감도를 조정할 수 있다. 흡기의 목표는 곧 일회호흡량(tidal volume, TV)이며 원하는 일회호흡량을 만들기 위하여 흡기시 목표 흡기유량(volume limit [실제로 flow])을 설정하는 것이 용적조절환기, 흡기시 목표 기도압(pressure limit)을 설정하는 것이 압력조절환기이다. 흡기의 종료는 자발호흡이 있다면 최대 흡기 대비 흡기유량 비율(inspiratory cycle off, %)로 조절하고 자발호흡이 아니라면 호흡수와 흡기호기비(inspiratory-to-expiratory ratio)에 따라 결정되는 흡입 시간에 따라 정해진다. 최고기도내압(peak airway pressure, Ppeak)은 폐와 흉벽의 저항력과 탄성력을 극복한 흡기 중 최고 기도압이며, 고원압력(plateau pressure, Pplat)은 폐포가 펴지면서 환기가 최대로 이루어지는 흡기말의 기도압이다. 용적조절환기에서 고원압력은 최고기도내압보다 낮지만, 압력조절환기에서 최고기도내압은 곧 고원압력이다.
각 환기 양식에 따라 나타나는 기본 그래프 파형은 Fig. 3과 같으며 특징적 파형으로 환기 양식을 역으로 유추할 수 있다. 보통 시간당 압력, 기류, 용적 변화를 각각 보여주는 pressure, flow, volume scala 그래프와 서로 관계를 보여주는 용적-압력, 기류-압력 루프(volume-pressure, flow-pressure loop) 그래프 중 선택하여 화면에 배치할 수 있다. 그러나 기계환기기의 제조사에 따라 환기 설정의 양식 이름 및 설정 요인에 차이가 있을 수 있으며, 사용하는 기계환기기에서 구동 가능한 양식의 특징을 파악하고 환자의 상태에 맞게 적용해야 한다(Fig. 4).
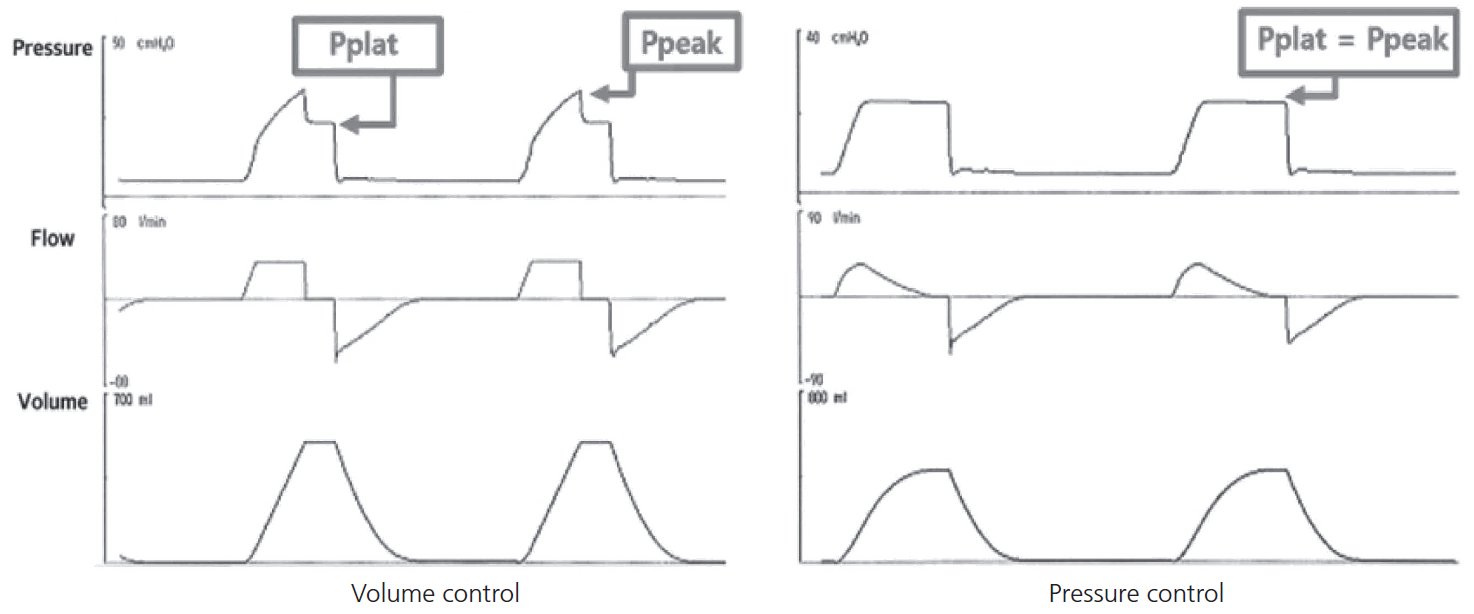
Basic waveforms of volume control and pressure control mode. Pplat, plateau pressure; Ppeak, peak airway pressure.

Actual monitor display of mechanical ventilator in different manufacturers. (A) Servo-I (MAQUET, Rastatt, German). (B) G-5 (Hamilton Medical, Bonaduz, Switzerland).
1) 뇌손상 환자에서 폐보호환기전략
폐보호환기전략(lung protective ventilation strategy)은 급성호흡곤란증후군(acute respiratory distress syndrome, ARDS)을 대상으로 사망률을 줄이기 위하여 제안되었으나[3,4] 현재는 기계환기 중인 환자에서 널리 적용되고 있다 [5-7]. 중요한 원칙은 (1) 저용적 일회호흡량(low tidal volume): 4-8 mL×성별과 키로 계산한 예측 체중(kg)=목표 일회호흡량, (2) 고원압력 ≤30 cmH2O, (3) 적절한 호기말양압(positive end expiratory pressure, PEEP)이며 중증의 ARDS에서 저용적 일회호흡량과 고원압력 제한으로 인한 호흡성 산증은 허용적 고탄산혈증(permissive hypercapnia)으로 pH 7.30까지 교정하지 않는다 [8].
두개내압 상승의 우려가 있는 신경계 중환자의 경우 고탄산혈증과 산증에 의한 뇌혈류량 증가로 두개내압 상승이 악화될 수 있어 허용적 고탄산혈증을 그대로 적용하기 어렵다. 그러므로 폐손상이 심하지 않고 두개내압 상승의 우려가 있는 환자는 정상 pH 및 이산화탄소 분압 범위 이내에 맞추어 일회호흡량(6-8 mL/kg) 및 호흡수를 조절한다.
호기말양압은 호기시 폐포허탈을 예방하고 말단 기도의 재개방을 도와 폐포동원(alveolar recruitment)을 유지하여 가스 교환을 증가시키므로 산소 전달이 중요한 기계환기 중인 뇌손상 환자에서 반드시 적용해야 한다. 호기말양압이 10 cmH2O 이하면 두개내압에 영향이 없고[9], 이미 두개내압 상승이 있거나[10] 또는 심한 폐손상으로 폐순응도가 감소하면 호기말양압을 올려도 두개내압을 상승시키지 않는다는 보고도 있어[11] 폐손상이 심하지 않다면 10 cmH2O까지 적용할 수 있다. 폐손상 정도를 고려하여 그 이상의 PEEP를 사용할 수 있으나 뇌압뿐 아니라 뇌 산소 전달의 측면에서 산소포화도, 뇌관류압을 고려하여 신중한 조절이 필요하다. 자세한 내용은 2016년 대한중환자의학회 ARDS 지침[12] 및 본 학회지 종설에서 참고할 수 있다[13].
그러나 실제 임상에서 뇌손상 환자의 기계환기는 폐뿐 아니라 기도, 호흡근, 호흡중추 등 환기 과정의 다양한 문제가 복합되어 조절하기 쉽지 않다. 신경학적 감시를 위하여 두개내압 측정 및 조직산소화 평가와 함께 기계환기기에서 보여주는 수치와 그래프 파형이 주는 정보를 면밀히 감시하여야 하며 기본적인 일회호흡량, 기도압 외에 참고할 수 있는 지표는 다음과 같다.
2) 폐 관련: 순응도(compliance)와 용적-압력 루프(volume-pressure loop)
순응도는 탄성의 역비이며 폐와 흉벽을 포함한 흉부 정적순응도(static compliance)는 용적조절환기 동안 일회호흡량을 압력 변화(driving pressure; Pplat-PEEP)로 나눈 값이다. ARDS처럼 순응도가 떨어진 폐는 일회호흡량이 같아도 폐포동원에 필요한 압력 변화, 즉 driving pressure가 15-19 cmH2O보다 크면 사망률이 증가한다고[14] 알려져 있어 저용적 일회호흡량과 함께 최적의 일회호흡량을 설정하는 참고 기준으로 최근 주목받고 있다. 또한 호기말양압을 올려 폐순응도가 증가하지 않고 감소한다면 폐포과다팽창을 의미하므로 적절한 호기말양압을 판단하는 기준이 되기도 한다. 뇌손상 환자에서 호기말양압을 올릴 때 폐순응도가 감소한 환자는 뇌압이 증가한 반면, 폐순응도가 증가한 환자는 가스 교환의 호전으로 이산화탄소 분압의 감소와 함께 뇌압도 변화가 없어[15] 두개내압 상승의 우려가 있는 환자의 호기말양압 설정에 참고할 수 있다. 최근 개발된 대부분의 기계환기기에서 순응도는 수치로 확인할 수 있으며, 정상 범위는 약 50-100 mL/cmH2O이고, 용적-압력 루프를 통해서도 순응도의 변화를 확인할 수 있다(Fig. 5).
3) 기도 관련: 자가호기말양압(auto-PEEP), 공기누출(air leak)과 기류-압력 루프(flow-pressure loop)
환자와 기계환기기 간 연결로 전체를 기도의 연장으로 생각할 수 있으며, 기도 관련 문제가 의심되면 환자와 기계환기기 양쪽을 같이 확인해야 한다. 기도내 분비물이나 기관지 연축 등으로 기도내 직경이 좁아지거나 말단 기관지가 닫히는 경우에 기도내 저항이 증가할 수 있으며 자가호기말양압이 나타날 수 있다. 자가호기말양압은 호흡일을 증가시키고 폐포과팽창을 일으켜 폐손상을 악화시키며 기관지 폐색의 조기 징후일 수 있으므로 기계환기기 그래프 파형을 통하여 발견하면 반드시 원인을 찾고 해결해야 한다. 특히 천식, 만성 폐쇄성 폐질환의 기저질환을 가진 환자에서 일회호흡량을 늘리고 호흡수를 줄여 호기를 길게 유지하여 자가호기말양압의 발생을 줄이는 것이 중요하다. 자가호기말양압은 기류 파형이나 기류-압력 루프에서 쉽게 찾을 수 있다(Fig. 6).
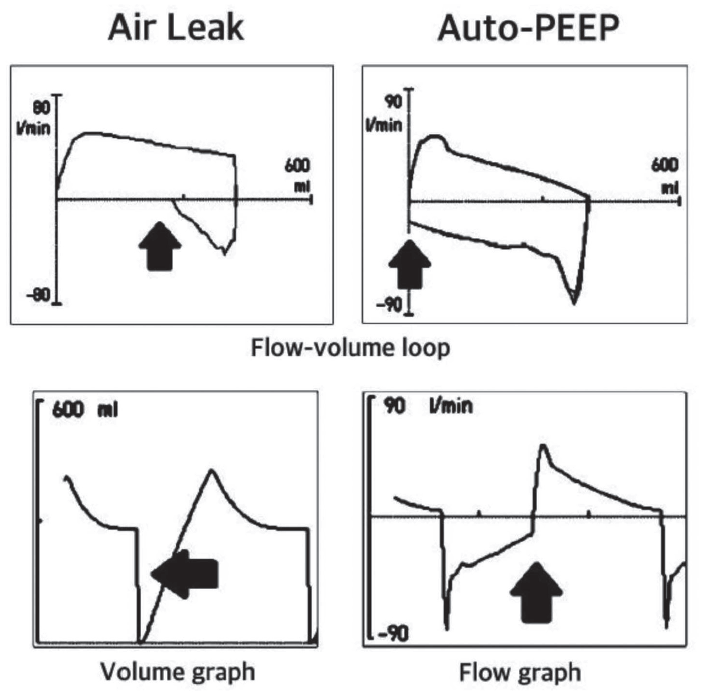
Ventilator waveforms of air leak and auto-PEEP. Difference between air leak and auto-PEEP on flow-pressure loop. It is important to make sure that the initiation of inspiration and termination of expiration cross at the same point on the flow-pressure loop. Air leak and auto-PEEP are seen in the volume graph and flow graph, respectively. PEEP, positive end expiratory pressure.
기계환기는 환자에서 기계환기기까지 연결된 기도 중 외부와 차단되지 않은 부분이 있으면 공기의 누출이 일어나 충분한 일회호흡량이 유지가 안되거나, 환자의 호흡과 상관없는 기류가 발생하여 기계환기기가 자발호흡 노력으로 잘못 감지할 수 있다. 공기 누출은 용적 파형 또는 기류-압력 루프를 통하여 쉽게 확인할 수 있으며(Fig. 6) 환자, 기관내 삽관튜브, 연결로, 기계환기기 등 모든 곳에서 누출 부위를 찾아야 한다.
4) 환자-기계환기기 비동시성(asynchrony)
환자-기계환기기 간 호흡주기가 맞지 않으면 환자의 불편감과 호흡일이 증가하며 폐손상의 악화로 기계환기 적용 기간의 증가 및 중환자실 사망률 증가 등 불량한 예후를 갖게 된다[16]. 특히 뇌손상 환자는 불규칙한 호흡주기를 가지는 경우가 많으므로 추가적인 폐손상을 줄이기 위하여 비동시성을 감시해야 한다. 기계환기를 적용 후 비동시성을 줄이려면 적절한 진정이 필수적이며 자발호흡 평가를 위하여 자발호흡시도(spontaneous breathing trial, SBT)를 정기적으로 시행해야 하나 두개내압 상승의 우려가 있는 환자에서는 신중히 시행되어야 한다.
(1) 흡기 비동시성
① 유발 비동시성(trigger asynchrony): 유발실패(missed trigger), 자가유발(auto-triggering)
환자의 흡기 노력을 기계환기기에서 감지하지 못하여 흡기 시작이 되지 않는 것을 유발실패라고 하며 호기에서 기류 파형의 상향굴곡(positive deflection)이 있으나 호흡주기가 시작되지 않은 것으로 알 수 있다. 호기 시간이 충분하지 않으면 상대적으로 기도저항이 높은 것처럼 공기가 다 빠져나가지 못하여 자가호기말양압이 발생하는데 이 압력차를 극복할 만큼 흡기 노력이 충분하지 않거나 유발 민감도가 너무 높을 때 발생한다.
자가유발은 환자의 흡기 노력과 상관없이 기도내 물이나 기도 누출 등에 의하여 유발이 시작되는 것으로 유발 민감도가 높은 유량 유발 방식에서 더 잘 생긴다. 원인을 제거하고 유발 방식을 변경한다(Fig. 7A).
② 유량 비동시성(flow asynchrony): 공기부족(air hunger), 유량과다(overshooting)
용적조절환기에서 설정된 흡기유량이 환자의 요구량보다 부족한 경우 더 많은 공기를 끌어당기기 위하여 호흡근을 과다하게 사용하여 생긴다. 호흡일을 증가시키고 불편감을 주기 때문에 압력조절환기로 변경하거나 흡기유량을 충분히 올려준다. 흡기유량이 과도하게 빠르거나 압력조절환기에서 유량 속도 증가 시간(rise time)이 너무 짧으면 초기 흡기시 기도압이 급격히 상승하는 overshooting이 발생하여 불편감을 준다(Fig. 7B).
③ 호흡종료 비동시성(termination asynchrony): 조기종료(premature termination), 이중유발(double-triggering), 종료연장(delayed termination)
조기종료는 기계환기의 흡기 시간이 환자가 원하는 것보다 짧을 때 생기며 호기에서 기류 파형에 상향굴곡이 있다. 호흡이 새로 시작되면 이중유발이 된다. 지속되면 폐의 압력손상 또는 용적손상을 일으킬 수 있다. 종료연장은 반대로 기계환기의 흡기 시간이 환자가 원하는 것보다 길 때 생기며 흡기말 압력파형에서 압력증가(pressure spike)가 생긴다(Fig. 7C).
(2) 호기 비동시성: 자가호기말양압
자가호기말양압은 임상적으로 가장 중요한 호기 비동시성이며 기도저항의 증가 또는 상대적 호기 시간의 단축에 의하여 나타날 수 있다. 압력차를 극복할 수 있는 호기말양압을 추가로 주거나 기도저항의 원인을 해결하거나, 흡기호기비나 호흡수를 조절하여 호기 시간을 충분히 늘려주면 해결할 수 있다.
2. 다양한 임상상황에서 그래프 파형의 감시
1) 호흡근 마비
진행하는 호흡근 마비로 기계환기가 필요한 길랭-바레증후군이나 중증 근육무력증 등 신경면역질환, 호흡근 마비가 올 수 있는 C5 이상의 척수염 또는 외상성 척수손상은 병의 경과에 따라 기도 확보를 하고 근력이 회복될 때까지 호흡일을 줄여주는데 초점을 맞추어야 한다. 의식과 자발호흡이 있기 때문에 적절한 진정과 함께 다양한 비동시성에 대한 감시와 조절이 필요하다. 호흡근 마비가 진행하면 유발실패가 있을 수 있으므로 압력보조환기보다 통제환기가 분당 환기량을 유지하는데 적합하나 비동시성을 감시해야 한다. 통제환기를 유지하는 동안 정기적으로 자발호흡을 확인해야 하지만 일반적인 기계환기 이탈 기준을 적용하여 기계환기를 종료하면 호흡근 피로로 인하여 수 시간 후 호흡곤란이 올 수 있다. 비침습적 기계환기는 신경면역질환에서 효과적이지 않다[17,18]. 용적조절환기에서 유량 부족이 관찰되면 유량을 높이기 위하여 일회호흡량을 조절하거나 흡기호기비를 조절하여 흡기 시간을 줄인다.
2) 두개내압 상승 시 폐손상
심한 뇌손상으로 인한 급격한 두개내압 상승은 이차 뇌손상의 기전 중 하나이자 급성 폐손상의 원인이 될 수도 있다. 초기 발생 후 24-48시간 내 대부분 호전되는 신경성 폐부종(neurogenic pulmonary edema)뿐 아니라 장기적인 중환자실 예후와도 밀접한 ARDS, 기계환기기관련폐렴(ventilator associated pneumonia, VAP) 등은 뇌보호와 폐보호의 원칙을 모두 잘 고려하여 치료하여야 한다. 폐보호환기전략의 내용과 뇌손상 환자에서 적용은 위 내용을 참고한다.
3) 불규칙한 호흡
뇌손상 환자에서 두개내압 상승 또는 호흡중추에 이상이 생기면 다양한 호흡양상을 나타내는데 흔한 것이 반복적인 무호흡 또는 과호흡이다. 과호흡으로 인한 저탄산혈증은 외상뇌손상, 거미막밑출혈 등 심한 뇌손상에서 불량한 예후를 시사한다[19,20]. 무호흡이 주기적으로 나타나는 경우 분당 환기량과 정상 이산화탄소 분압이 유지될 수 있도록 통제환기, 동조간헐필수환기 또는 뒷받침환기(backup ventilation)를 충분히 설정한 보조환기를 사용할 수 있다. 그러나 과호흡이 같이 나타나는 경우 강력한 자발호흡을 기계환기만으로 완전히 통제할 수 없으므로 충분한 진정으로 우선 저탄산혈증을 조절하며 압력보조환기 등으로 호흡일을 보조하고 비동시성을 줄이는데 초점을 맞춘다. 하지만 중등도의 폐손상이 나타나면 근육이완제를 조기에 사용하여 폐보호환기전략에 맞게 일회호흡량을 조절하는 것이 도움이 된다. 폐손상이 나타나기 전 근육이완제를 써서 과호흡을 조절하는 것은 신경학적 평가를 지연시켜 뇌손상 악화의 발견시기를 놓칠 수 있으므로 현재로써 추천되지 않는다.
결 론
중환자실 치료가 필요한 뇌손상 환자에서 기계환기는 중요한 치료이며 추가적인 뇌손상과 폐손상을 줄이기 위하여 환자 개개인의 상태에 따른 적절한 기계환기 설정뿐 아니라 지속적인 기계환기의 감시와 조절을 위하여 기계환기의 그래프 파형의 의미를 알고 해결하려는 노력이 필요하다.