증 례
74세 남자가 3주 전에 갑자기 생긴 하반신마비를 주소로 내원하였다. 증상은 악화나 호전 없이 지속되었으며, 마비 1주 전에는 배뇨 장애가 있어 유치도뇨관 삽입술을 시행받고 이를 유지하고 있었다. 하반신마비와 함께 하반신 감각 저하도 동반되었으나, 등이나 허리의 통증은 없었다고 하였다. 환자는 15년 전 고혈압을 진단받아 항고혈압제를 복용하고 있었다. 35갑년의 흡연력이 있었으나, 자가면역질환 및 외상 병력은 없었다.
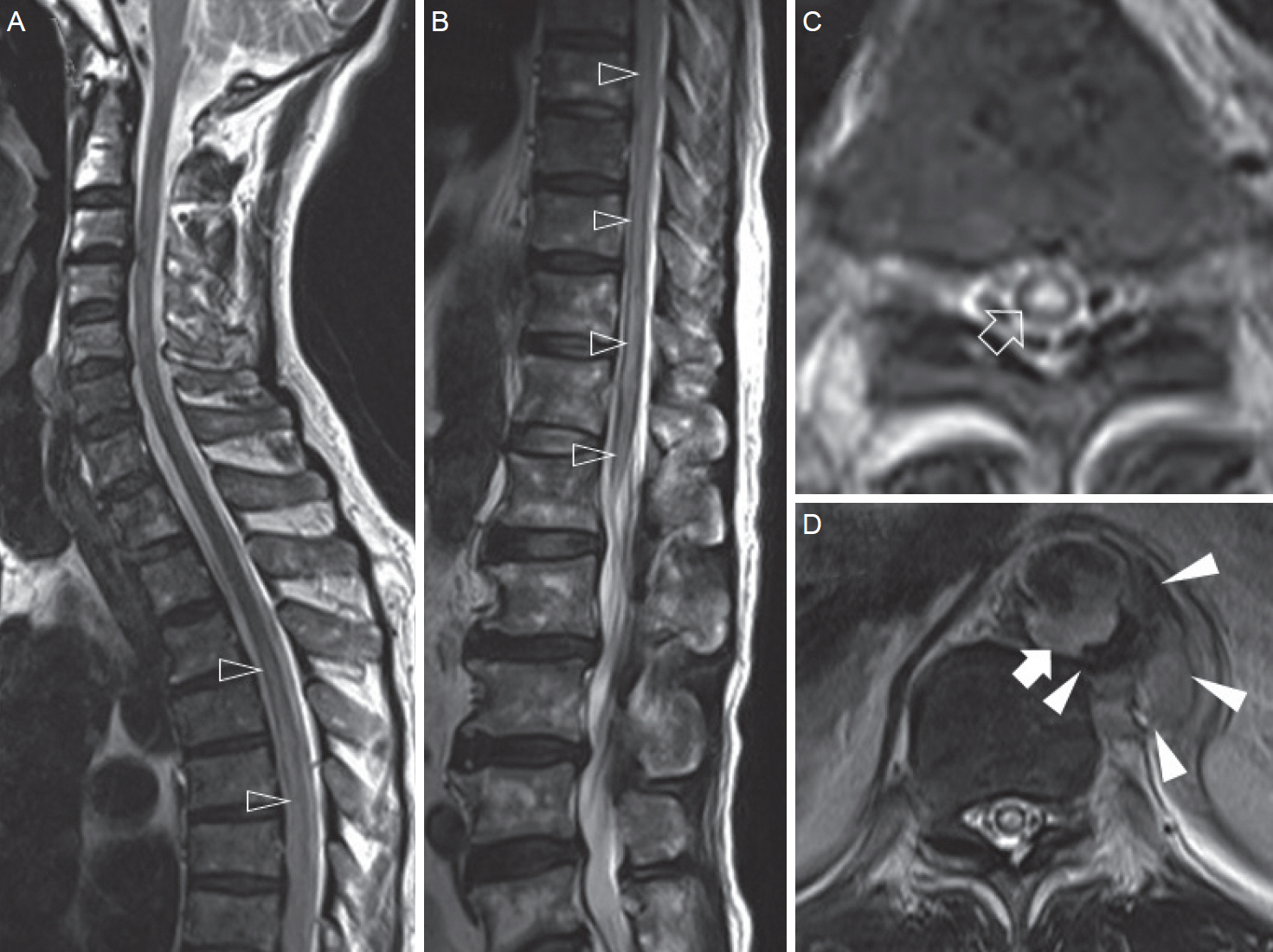
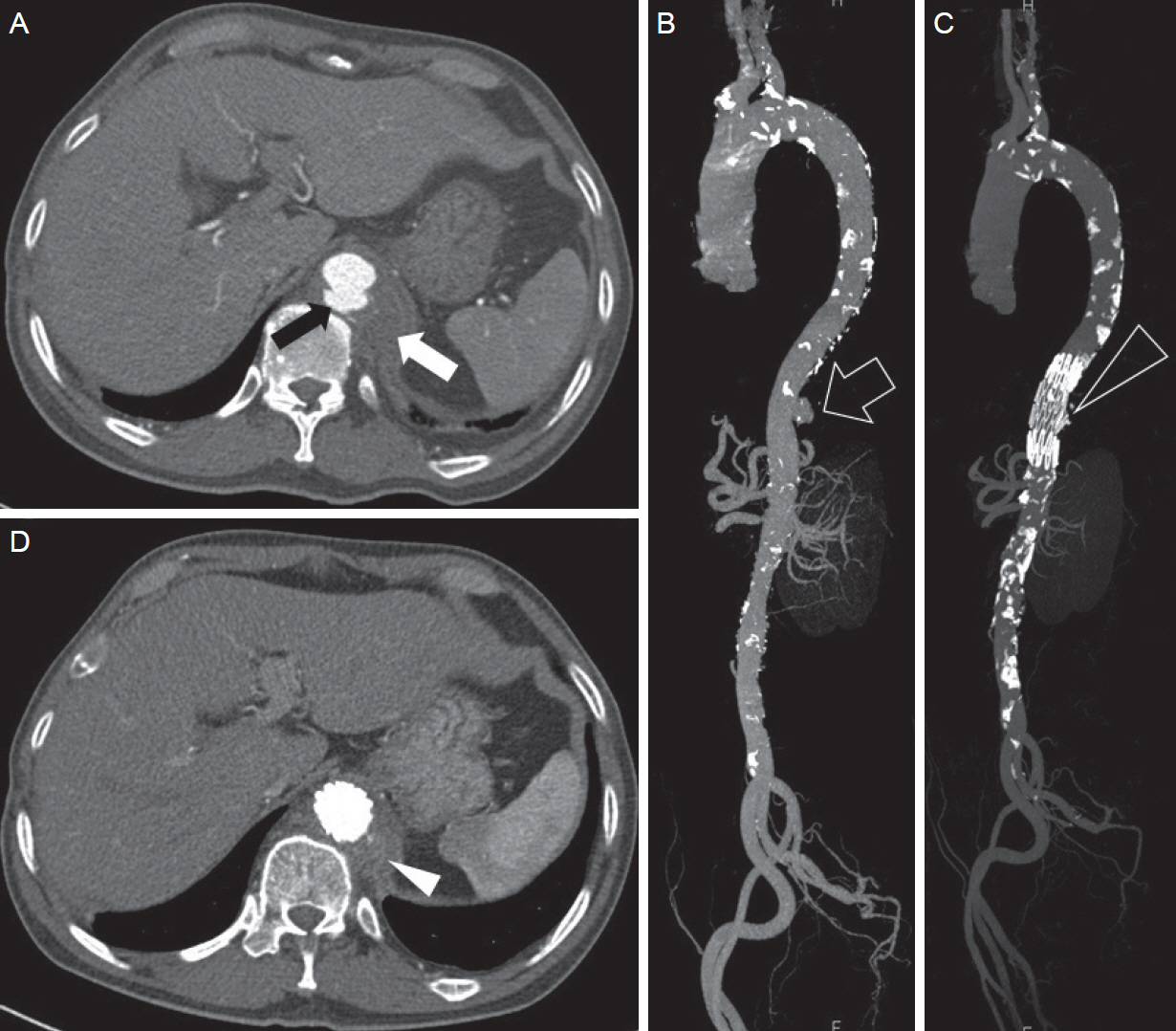
진찰상 근력은 양쪽 다리가 Medical Research Council (MRC) 2등급이었다. 침 통각, 촉각 감각 검사에서 양쪽 제1 허리 척추 수준 아래로 침 통각 및 온도 감각이 감소되어 있었다. 양쪽 무릎반사와 발목반사도 감소(1+)되어 있었으나 양쪽 팔에서 건반사는 정상이었고, 바빈스키징후는 양쪽에서 보이지 않았다. 혈압 136/79 mmHg, 맥박 64회/분, 호흡 16회/분, 체온 36.7°C였고, 혈액검사상 온혈구계산(complete blood count)에서 혈구 수치는 정상이었다. 간기능검사, 콩팥기능검사, 혈청 rapid plasma reagin 및 사람 면역결핍바이러스 항체검사들도 정상이었다. 척추 자기공명영상(magnetic resonance imaging, MRI)의 T2강조영상에서 제3 흉부 척수 이하 부위에 광범위 고신호병변이 있었다(Fig. 1A-C). 이와 함께 제10-11 흉추 수준의 흉부대동맥 뒤로 고신호강도의 종괴처럼 보이는 병변과 그 주위에 혈종도 보였다(Fig. 1D). 대동맥전산화단층혈관조영(computed tomography angiography, CTA)검사에서 종괴는 관통죽상경화성궤양(penetrating aortic ulcer, PAU)으로 인한 흉부대동맥류(3.2 cm)의 절박파열(impending rupture)로 확인되었다(Fig. 2A, B). 환자 증상은 이로 인한 척수경색과 관련된 것으로 생각하고, 원위흉부대동맥에서 복강위복부대동맥까지 길이 80 mm, 내경 28 mm의 흉부대동맥내 스텐트 이식편(Zenith TX2®; William Cook Europe, ApS, Bjaeverskov, Denmark)을 이용한 혈관내동맥류재건술(thoracic endovascular aortic repair, TEVAR)을 시행하였다. 시술 한 달 후의 추적 CTA에서 PAU 병변은 호전되었고, 동맥류 및 그 주위의 혈종은 감소되었다(Fig. 2C, D). 진찰에서는 양쪽 다리 근력이 MRC 4+등급이 되어 걸어서 퇴원하였다. 하지만 배뇨 장애는 남아있어, 유치도뇨관은 계속 유지하게 되었다.
고 찰
척수경색의 빈도는 뇌경색의 1%로 드물게 발생한다고 알려져 있지만, 다리마비 및 대소변실금 등 심각한 장해를 야기하는 경우가 많다[1]. 척수경색은 특발성으로 발생하는 경우가 가장 흔하고, 흉복부대동맥 수술 합병증 및 전신동맥경화도 이의 흔한 원인이며, 대동맥박리 또는 대동맥류 등도 원인이 될 수 있다[2].
본 환자의 척추 MRI에서는 광범위 척수병증을 시사하는 소견 외에 원위흉부대동맥 부위로 종괴처럼 보이는 병변이 발견되었고, 대동맥 CTA 시행 후 PAU에 의한 동맥류 절박파열로 진단하여, 이로 인하여 발생한 척수경색이라 판단하였다. PAU는 동맥경화 병변의 궤양이 혈관 바닥판(basal lamina)을 뚫고 나가 중막 또는 외막하혈종을 유발하는 것으로, 주로 하행대동맥에서 동맥류를 형성하고 파열로도 진행하는 경우도 있어, 신속한 치료를 요하는 상황으로 알려져 있다[3].
척수의 혈액 공급은 크게 주로 척추동맥에서 기시하는 전척수동맥(anterior spinal artery)과 후척수동맥(posterior spinal artery) 그리고 대동맥에서 분지되는 동맥으로부터 형성되는 신경뿌리척수동맥(radiculo-medullary artery)이 담당하지만, 대부분은 신경뿌리척수동맥에 의한다[4]. 신경뿌리척수동맥은 전신경뿌리척수동맥과 후신경뿌리척수동맥으로 분지되며, 이 동맥들은 각각 전척수동맥과 후척수동맥으로 연결된다. 전신경뿌리척수동맥 중 가장 큰 동맥을 Adamkiewicz동맥이라 하는데, 이는 주로 제9-12 흉추 수준 대동맥에서 분지되는 늑간동맥에서 기원하는 혈관이며, 흉부척수에서 척수원뿔까지 광범위한 척수 부위에 혈액 공급을 담당한다[4]. 본 환자의 동맥류는 PAU에 의한 것으로, 제10-11 흉추 수준에 위치해 있었다(Fig. 2A, B). 따라서 동맥류 주변의 혈종 등에 의하여 늑간동맥이 폐색됨에 따라 Adamkiewicz동맥의 혈류 공급이 차단되어 척수경색이 생겼을 것으로 판단된다. Adamkiewicz동맥은 주로 척수 앞 2/3 영역의 혈액 공급을 담당하므로[4], 이 동맥 내의 혈류 장애로 인한 척수경색 시에는 주로 앞뿔(anterior horn)을 포함한 척수 앞쪽 부위에 신호 이상이 MRI에서 나타나게 된다. Mawad 등[5]은 흉복부대동맥류수술 후에 발생한 척수경색 환자들의 영상 소견을 분석하였는데, 24명 중 12명의 척수 MRI 횡단영상에서 척수의 앞쪽 부위뿐 아니라 다른 부위도 침범한 광범위 병변이 있었다. 이들은 전척수동맥영역의 척수경색시 앞뿔을 포함한 회질의 괴사가 빨리 진행하고, 경색이 심하거나 시간이 지날수록 척수 앞쪽 부위의 병변이 진행하여 광범위한 병변이 생길 수 있다고 주장하였다. 본 환자의 진찰상 양쪽 다리 근력은 MRC 2등급으로 비교적 심한 하반신마비를 보였으며, 증상 발생 후 3주 정도 지난 시점에서 MRI가 시행되어 환자의 척수 MRI 횡단영상에서 보이는 광범위 병변은 척수경색에서 충분히 보일 수 있는 소견으로 판단할 수 있겠다.
흉부대동맥류의 치료 방법은 동맥류 부위를 제거하고 인조혈관으로 치환하는 수술적 치료 방법과 중재적 시술인 TEVAR가 있다. TEVAR는 1994년 Dake 등[6]에 의하여 처음 시도되었고, 98%의 높은 대동맥류 치료 성공률을 보이고 있다. 치료 관련 사망률도 TEVAR의 경우 1.9-2.9%로 수술의 5.7-11.7%에 비하여 낮다는 결과들이 있다. 또한 신속히 시행할 수 있고, 시술 시간도 수술 시간보다 짧아 현재 임상에서 널리 이용되고 있다[7]. TEVAR는 동맥류 부위를 스텐트 이식편으로 덮어 동맥류 부위로의 혈류 흐름을 차단하여 동맥류의 확장 및 파열을 방지하는 역할을 하는데[8], 치료 후 본 환자의 동맥류의 크기가 줄어들었다(Fig. 2C, D). 따라서, TEVAR 후에 폐색된 늑간동맥이 재개통되었고, 이로 인하여 Adamkiewicz동맥으로의 혈류 공급이 원활해져 환자의 증상이 호전되었으리라 추측된다.